肖海娟医生的科普号
- 引用 甲状腺癌术后须知
甲状腺癌的治疗方式和过程,最主要的就是手术,其次就是术后的药物抑制治疗,小部分患者还需要做放射碘治疗,术后的随访也是很重要的内容。甲状腺癌一般不需要做放疗和化疗,除非特殊类型的,相对罕见。一、复发的风险二、药物抑制治疗1.由于甲状腺癌的生长和身体内的促甲状腺激素(TSH)水平有关,因此可以服用左甲状腺素片(优甲乐)来降低TSH水平,让机体处于轻度甲亢的状态,抑制术后癌症复发。2.术后TSH<2.0mU/L者,相关的死亡率和复发率比TSH>2.0mU/L明显减少,因此TSH 2.0mU/L是最基本的药物抑制目标。3.不同甲状腺癌人群的抑制目标见下图,达到满意调整目标之前需要每6周复查一次甲功能,稳定后可间隔3-6月再复查。4.老年人和绝经期后的女性,考虑到长期抑制治疗引起心血管和骨质疏松甚至骨折的风险,可酌情降低药物抑制的目标,并加用调整心率的药物。5.抑制治疗的时间一般以5年为界,中低危的人群观察5年无异常可停药或维持甲功正常即可。高危的人群5年后检查无复发,TSH可放宽为 0.5—2.0 mU/L。6.长期进行术后抑制治疗的人群,应每天补钙1200mg,通常饮食中钙含量800mg,中老年人需要另外补充,年轻人可不用或者少量补钙。三、放射碘治疗1.放射碘治疗的原理是:人体内主要是甲状腺癌组织摄取放射源,因此可以消灭甲状腺癌,而对正常人体组织影响很小。2.放射碘治疗目的就是为了配合手术,利用放射线清除人体内极少数剩余的甲状腺、肿瘤和转移淋巴结。手术就是“扫地”,还有灰尘和污渍需要放射碘来“拖地”。3.是否需要放射碘治疗,需要手术医生根据手术中所见和病理结果,作出提议。而核医学科的医生会根据检查结果和手术医生的意见,作出是否进行放射碘治疗的最后决策。4.通常需要1-2次放射碘治疗即可,两次间隔时间4—12个月,每次为住院5天,口服放射碘药水。5.放射碘治疗之前需要停用左甲状腺素片20天,低碘饮食。6.只切除一侧甲状腺的患者,无法、通常也无需进行放射碘治疗。四、随访观察方法1.随访观察的主要目的是检查有无术后复发,方法是抽血检查Tg(甲状腺球蛋白)和影像学(B超、CT)检查。2.Tg是甲状腺组织特有的,因此甲状腺全切除后测定的Tg越低越好(<0.2ug/L),说明人体内没有甲状腺和肿瘤存在。如果只切除一侧甲状腺,Tg数值的意义需要和影像学检查结果一起来评判。术后5年内应每隔半年检查一次Tg,稳定后可每年检查一次。由于Tg水平与TgAb抗体有关,因此需要同时检测。3.甲状腺癌最多见的是乳头状癌,术后复发主要是表现在颈部出现淋巴结转移、肿大,B超医生可以发现可疑的淋巴结肿大,若淋巴结大于8mm,可行淋巴结穿刺和Tg测定明确是否转移,确诊后可考虑再次手术切除。术后颈部的B超第一次复查是术后6个月,术后5年内应每年检查一次,复发风险高或发现小的可疑淋巴结,可半年检查一次。其次,甲状腺癌术后可能出现肺部的转移结节,由于结节一般很小,需要胸部CT检查才能发现,对于复发风险很小以及Tg很低或者稳定的患者,胸部CT可以不用每年检查。4.甲状腺滤泡癌的患者,最容易发生骨转移,几乎不会出现颈部淋巴结转移。除了监测Tg之外,全身骨扫描可术后第1年、第3年、第5年做,检查无异常可不用再检查。五、复查结果解读及处理——以上内容主要来自《分化型甲状腺癌术后管理中国专家共识(2020版)》
檀谊洪 主任医师 佛山市南海区人民医院 甲状腺外科2597人已读 - 引用 认识结直肠神经内分泌肿瘤
目前,结直肠癌已逐步被大家所熟悉。然而提到一类特殊的结直肠肿瘤,即结直肠神经内分泌肿瘤,广大病友及家属却经常充满困惑。这里我们做一个简单的介绍。神经内分泌肿瘤(Neuroendocrine tumors,NETs)是一类起源于神经内分泌细胞的肿瘤。结直肠为神经内分泌肿瘤的高发部位,发病率占所有神经内分泌肿瘤的17.7%。在最近30年中,结直肠神经内分泌瘤的发病率增长超过10倍。其男女发病率基本相当。由于神经内分泌肿瘤可产生5-羟色胺代谢产物或多种激素,可将其分为功能性和非功能性两大类。功能性神经内分泌肿瘤主要表现为肿瘤分泌的激素类物质所引起的各种临床症状,如皮肤潮红、腹泻、哮喘、低血糖、糖尿病等。非功能性神经内分泌肿瘤主要表现为非特异性的消化道症状。结直肠神经内分泌肿瘤的临床症状多不典型,与结直肠癌类似(如排便习惯改变、便血、黑便、腹胀、腹痛、恶心、呕吐、食欲不振、体重减轻等),有功能的肿瘤非常少见。结直肠神经内分泌肿瘤尚缺乏特异性的血清肿瘤指标。其诊断主要依据结肠镜、活检或手术病理。其肿瘤组织内可特异性表达嗜铬素A,突触素,神经元特异性烯醇化酶等标志物,临床上可以作为诊断的重要指标。结直肠神经内分泌肿瘤的诊断是依据2010年WHO分类系统。NET 1级(G1,类癌,核分裂象数<2 10=""net="">20/10 HPF,Ki67增殖指数>20%,包括小细胞癌、大细胞癌、混合型腺神经内分泌癌)。手术切除是治疗结直肠神经内分泌肿瘤的主要手段。对于病灶小于1cm的G1和G2、没有淋巴结转移、没有肌层侵犯的结直肠神经内分泌肿瘤,可采用局部切除,达到根治,不需要太紧张。对于病灶1~2cm的G1和G2、没有淋巴结转移、伴或不伴肌层侵犯(未穿透肌层)的结直肠神经内分泌肿瘤可行局部扩大切除术。对于>2cm的结直肠神经内分泌肿瘤或活检病理提示结直肠神经内分泌癌(G3),应按结直肠癌行根治性手术。对于结直肠神经内分泌癌(G3),即使肿瘤已经发生转移,也应尽可能地切除原发灶、转移灶及清扫淋巴结,以达到降低瘤负荷、解除症状的目的,提高患者的生存质量。化疗是治疗结直肠神经分泌肿瘤的一个重要手段,其中Ki-67是判断肿瘤细胞增殖活力的一个重要指标,Ki67>5%即应采取化疗。常用药物包括VP-16(依托泊苷)、顺铂、5-FU、阿霉素等。对于穿透肌层、或伴有淋巴结转移的直肠癌,可考虑局部放疗。少数类癌综合征患者术后使用生长抑素类似物(善龙等)辅助治疗,可能有理想疗效。结直肠神经内分泌癌的预后比相同分期的腺癌要差,尤其是小细胞癌的预后更差。
周海洋 副主任医师 上海长征医院 肛肠外科1.2万人已读 - 引用 乳腺结节知多少?
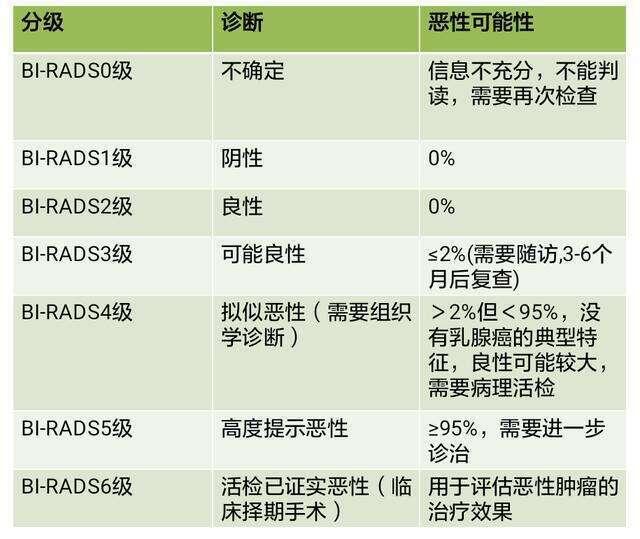
乳腺结节是乳腺癌吗? 近年来乳腺健康受到广泛关注,很多女性朋友会定期进行乳房自检或影像学检查(超声、钼靶、磁共振),一旦发现乳腺结节难免紧张害怕,甚至谈节色变,担心自己得了乳腺癌,乳腺结节就是乳腺癌吗? 1.何为乳腺结节? 乳腺结节通常是指发生于乳房的团块状的小病灶,较大的病灶通常称为乳房肿块,结节和肿块是两个相对的称谓。超声辨别乳腺微小肿块的能力较强,乳腺结节在超声报告中常见。 乳腺结节只是乳房疾病的一种表现形式,而不是疾病的诊断。乳腺疾病都可以表现为乳腺结节,如小叶增生、乳腺腺病、囊肿、肿瘤(纤维瘤、导管内乳头状瘤、脂肪瘤、叶状肿瘤、乳腺癌、淋巴瘤等)、结核等。乳腺结节不一定是乳腺癌。 2.乳腺结节需要手术吗? 乳腺疾病筛查方法是超声和钼靶,当二者检查结果不一致或不能有效评估病变时可选择磁共振进一步检查。为规范乳腺疾病诊疗美国放射学设立了乳腺影像报告和数据系统(BI-RADS)来评估乳腺病灶的性质。BI-RADS分级包括0~6级,分级越高恶性可能性越大。2级以小叶增生和单纯囊肿多见,一般不需要手术。3级良性可能,以纤维瘤、复杂囊肿、脂肪瘤多见,可短期随访观察;以下情况的3级结节建议积极手术。a.短期内长,b.大可以摸,c.年龄40岁以上,d.有乳腺癌,卵巢癌等恶性肿瘤病史或家族史,e.未生育,未哺乳,f.准备人工受孕,g.焦虑型患者,自己强烈要求手术等。而4级及以上的结节有恶性,可能建议及时手术。值得注意的是0级需要结合其他检查进一步评估病灶性质。 3.乳腺结节需要吃药吗? 排除了恶性可能性的结节,若伴有乳房疼痛不适可适当服用中成药,缓解症状;无疼痛不适症状可不服药。考虑炎症时,可服用抗生素。 4.乳腺结节可以预防吗? 乳腺结节可能与内分泌紊乱、精神压力大、生活方式、婚育、基因等综合因素有关,目前确切的病因尚不清楚。建议针对乳腺癌的高危因素进行防控,提倡健康的生活方式,合理饮食,定期进行乳腺检查,鼓励有氧运动,避免滥用保健品及避孕药等。 发现乳腺结节不必慌张,应及时到乳腺科就诊,听取医生的专业建议。
 陈园园 主治医师 中国福利会国际和平妇幼保健院 乳腺科1910人已读
陈园园 主治医师 中国福利会国际和平妇幼保健院 乳腺科1910人已读 - 引用 阿帕替尼真的适合多种晚期癌症治疗
在靶向药物越来越多的当今,有一个国产靶向药物不得不提,就是阿帕替尼(艾坦)。阿帕替尼的靶点包括:VEGFR1、VEGFR2、VEGFR3、PDGFR-β、C-KIT、FGFR1和FLT3。看了这么多靶点,自然会有更多的适应症,特别是VEGFR1/2/3这三个靶点,本身就属于抗血管生成范围,国外对应此类靶点的药物也普遍有较多的适应症,比如卡博替尼、雷莫芦单抗、贝伐珠单抗、仑伐替尼、瑞格菲尼等。目前我国批准的阿帕替尼适应症是晚期胃癌,这也是国内唯一获得批准的晚期胃癌靶向药物。国外被批准的药物还包括雷莫芦单抗、曲妥珠单抗(HER2靶点)。在国内来说,晚期胃癌使用阿帕替尼的客观缓解率(ORR)为18.1%,总有效率(DCR)是63.6%。已经是效果非常不错的一种靶向药物了。上面提到阿帕替尼的多个靶点,以及国外类似药物是有多种适应症的,因此阿帕替尼也在进行相关病症的试验,具体包括:肝癌、非小细胞肺癌(非鳞)、结直肠癌、三阴乳腺癌。在晚期肝癌试验中:药厂设计的试验首要终点是疾病进展时间(TTP),次要终点是DCR、ORR、总生存期(OS)。本次试验是与安慰剂对比。在试验结束后发现阿帕替尼与安慰剂相比,只是略有进展但没有统计学上的意义。对比目前国内已经批准的晚期肝癌靶向药物包括:索拉菲尼和仑伐替尼,除此之外国外还有瑞格菲尼和PD-1抑制剂。总的来说阿帕替尼获批的机会不高。在晚期非鳞非小细胞肺癌的试验结果是,,阿帕替尼组与安慰剂组的无进展生存期(PFS)相比为4.7月vs1.9月,优于安慰剂组2.8个月。不良反应可耐受,主要为蛋白尿、手足综合症、高血压。在目前非小细胞肺癌各种靶向药物和免疫药物大量获批的前提下,这个数据或许不足以吸引患者的注意。在晚期结直肠癌的试验显示:主要研究终点是ORR,次要指标是DCR、PFS、OS等。研究结果表明阿帕替尼用于晚期结直肠癌三线治疗有一定的效果,但样本数偏少,说服力不够。在晚期结直肠癌的药物中,贝伐珠单抗和西妥昔单抗,以及瑞戈菲尼都是强大的竞争者。对于三阴性乳腺癌的小规模试验结果是:主要研究终点是PFS(无进展生存期),次要指标是ORR、OS等。结果表明:阿帕替尼用于晚期三阴乳腺癌中位OS10.6个月,PFS3.3个月,ORR10.7%,常见3-4级不良反应有手足皮肤反应、蛋白尿、高血压、血小板减少等。虽然三阴乳腺癌的治疗药物少,但是今年已经有PARP药物用于晚期三阴乳腺癌的治疗,希望阿帕替尼能够有更好的试验结果证明来帮助获得批准。从以上的一些试验可以看出,对于阿帕替尼这种国产VEGFR的药物,主要还是用于胃及胃食管交接部的癌症治疗,针对其它病症的试验并未获得有说服力的成功。希望后续能有更好的试验结果。
匡山 中国人民解放军总医院第八医学中心 放疗科43人已购买 - 引用 靶向药物治疗肝内胆管癌
靶向治疗是针对肿瘤发生、发展中的关键靶点,通过特异性结合致癌位点干预信号转导,从而选择性地诱导肿瘤细胞坏死、凋亡或被免疫细胞吞噬。近年来,随着ICC基因图谱研究和对其分子病理机制认识的深入,对该病靶向治疗的研究迅速增加,但单独针对ICC开展的临床研究较少,大部分包含在胆道系统肿瘤中。(一)FGFR信号转导通路FGFR信号转导通路主要参与内皮细胞增殖和肿瘤新生血管形成,并与血管内皮生长因子(vascular endothelial growth factor,VEGF)具有互补和协同作用。最近有研究者发现,11%~45%的ICC患者存在FGFR2融合基因,但在肝细胞肝癌和肝外胆管癌中罕见,使其有希望成为治疗ICC的靶点。非选择性酪氨酸激酶抑制剂,如帕纳替尼(ponatinib)和帕唑帕尼(pazopanib),对存在FGFR2基因融合的晚期ICC患者有效。国外一项二期试验结果显示,泛FGFR抑制剂德拉替尼(derazantinib)治疗FGFR2融合突变ICC有一定效果。也有一期试验结果显示,被FDA批准用于尿路上皮癌的FGFR抑制剂厄达替尼(erdafitinib)对胆管癌有一定的应答率。TAS-120对部分FGFR2基因融合ICC的应答率也较好。(二)人表皮生长因子受体(epidermal growth factor receptor,EGFR)EGFR与ICC的发生密切相关,10%~32%的ICC患者过表达EGFR,EGFR对ICC患者的总体生存有负面影响。目前针对EGFR的靶向治疗药物主要有两种:一种是单克隆抗体,如西妥昔单抗(cetuximab)和帕尼单抗(panitumumab),另一种是小分子酪氨酸激酶抑制剂,如厄洛替尼(erlotinib)、拉帕替尼(lapatinib)和阿法替尼(afatinib)等。帕尼单抗联合吉西他滨、卡培他滨和奥沙利铂方案化疗的治疗试验结果反映联合用药可延长病人的无进展生存时间。厄洛替尼联合贝伐珠单抗(bevacizumab)可使部分晚期胆管癌患者生存获益。厄洛替尼联合GEMOX化疗也可使胆管癌患者的无进展生存时间延长(三)VEGFVEGF是调控肿瘤血管生成的主要细胞因子。约53.8%的ICC患者肿瘤组织过表达VEGF,且与不良预后密切相关。贝伐珠单抗联合GEMOX等未显示出足够的抗瘤效果。关于索拉非尼单药及索拉非尼联合厄洛替尼、吉西他滨或顺铂等多项结果均显示其治疗胆管癌的效果并不理想。凡德他尼(vandetanib)治疗胆管癌的二期临床试验结果提示可延长部分患者的无进展生存时间。(四)IDH基因突变IDH1/2基因突变在ICC中较常见,占所有ICC患者的18%~36%。被美国食品药品监督管理局(FDA)批准用于治疗IDH1突变的急性髓细胞性白血病的艾伏尼布(AG-120),是最早被研究应用于胆管癌的IDH1抑制剂。多激酶抑制剂达沙替尼(dasatinib)具有对IDH突变ICC的合成致死作用,可诱导细胞凋亡,评估该药对IDH突变ICC患者疗效的二期试验正在进行之中。另外,聚腺苷二磷酸核糖聚合酶(poly ADP-ribose polymerase,PARP)抑制剂可能与IDH1/2突变存在合成致死作用基于该结果,目前正在进行评价PARP抑制剂奥拉帕尼(dlaparib)对包括ICC在内的IDH突变肿瘤疗效的二期试验。(五)RAS-RAF-MEK-ERK通路RAS-RAF-MEK-ERK信号通路激活是胆管癌致病机制之一,其在胆管癌中常表达异常。ICC中KRAS基因突变率为8.6%~24.2%,其与ICC分期较晚、预后不良相关。BRAF则是KRAS的下游靶点,约1%的胆管癌有BRAF突变,在ICC中则为3%~5%。目前BRAF抑制剂治疗胆管癌的效果仅有零星报道,BRAF抑制剂维罗非尼(vemurafenib)单药的二期试验结果并不满意。司美替尼(selumetinib)是MEK1/2抑制剂。司美替尼单药治疗晚期胆管癌有一定效果;司美替尼联合吉西他滨、顺铂化疗可延长晚期胆管癌患者的无进展生存时间。BRAF和MEK双重阻断可能为BRAF突变的ICC提供新的治疗方法。(六)PI3K-AKT-mTOR通路与大部分恶性肿瘤相似,ICC中也表现为PI3K-AKT-mTOR通路的过度活性,并与患者的不良预后相关。MK2206是AKT的抑制剂,二期临床试验结果显示,其对化疗失败的晚期胆管癌患者并未显示良好效果。依维莫司(everolimus)是mTOR抑制剂,有一定疗效。在体外实验和临床前试验中,联合应用AKT和mTOR抑制剂均显示出良好的抗肿瘤活性,提示该治疗可能具有临床应用前景。(七)其他靶点ICC中可检测到ROS1融合基因,而ALK抑制剂可逆转ROS1融合基因的致癌作用。20%~58%的ICC表达MET,其过表达与不良预后相关。MET抑制剂tivantinib联合吉西他滨治疗胆道系统肿瘤的效果优于卡博替尼(cabozantinib)单药治疗,疗效也较好。总体而言,ICC的生长、侵袭和转移涉及多种分子和信号转导通路的调控,可选择的治疗靶点较多,分子靶向治疗是新的方向。目前已开展的许多基础和临床治疗研究,部分已显示良好的应用前景。但由于对ICC分子机制的认识尚不深入,当前靶向治疗的临床结果也多为来自于针对胆道系统肿瘤的二期单臂研究,且由于不同解剖部位胆道系统肿瘤之间存在分子病理和基因突变的不同,靶向治疗的效果也有较大差异。目前仍有待开展更多的针对ICC的多中心临床试验,进一步验证靶向药物对该病的有效性和安全性。
夏勇 副主任医师 海军军医大学第三附属医院 肝胆外科1万人已读 - 引用 房颤
心房纤颤(简称“房颤”,Af)是临床最常见的心律失常之一。房颤的发生会增加血栓栓塞、心力衰竭等并发症,加速病情进展及增加病死率。房颤引起的心悸、气短、乏力症状也严重影响了患者的生活质量。《ACC/AHA/ESC房颤处理指南2006》指出房颤治疗策略应体现个体化,对确诊房颤进行评估,以确定是阵发性、持续性还是永久性房颤,明确有关心脏或心外因素,综合分析后采取综合措施。虽然近年来房颤的射频消融有了飞速发展,但药物治疗仍然是一线治疗,有时甚至是唯一可行的方法。本文将就药物治疗进展简要综述。 控制心室率 控制房颤心室率常是治疗中第一个要考虑的问题。目标是将心室率控制在静息时60-80/min,中度活动后90-115/min。AFFIRM研究目标为静息时≦80/min,6min步行试验最大心率≦110/min或24h平均心室率、缺血性心脏病。对于无器质性心脏病的房颤或不伴心衰时可选用钙拮抗剂。洋地黄主要控制休息状态下的心室率,对于有心力衰竭伴快速性房颤首选。胺碘酮也有降低心室率作用,在其他药物控制无效或禁忌时可以考虑,一般作为二线用药。房颤心室率控制过程中值得注意的是,阵发性房颤不应该以洋地黄为唯一的心室率控制药物;对于尚未充分药物尝试控制心室率的患者不能进行房室结射频消融;对于伴心衰的患者不能使用非二氢吡啶类钙拮抗剂;有预激的患者不能使用洋地黄和非二氢吡啶类钙拮抗剂以免使心室率加快。 虽然有研究显示,控制心室率效果并不比药物维持窦性心律差,甚至在改善生活质量方面优于心律控制。但心室率的满意控制并不完全改善预后,对高危患者还需终生抗凝治疗。恢复并维持窦律 药物复律适用于那些时间不超过半年、心房不大、无结构性心脏异常、触发因素已经去除的阵发性或持续性房颤。 转复药物包括Ia类、Ic类和III类抗心律失常药,这些药物主要作用于心房,延长心房肌的动作电位时程和有效不应期。选用复律药物时需考虑房颤持续的时间,对于新发房颤选用Ic类药物效果较好;因为I类药物可能增加室性心律失常,Ic类药物具有负性肌力作用,故这类药物不宜用于器质性心脏病和左心功能不全者。对于发作7天以内的房颤适合转复的药物主要有伊布利特和普罗帕酮。胺碘酮则为IIa类选择。选用普罗帕酮时需注意是否房扑,对于房扑患者首先需要使用药物控制心室率,否则普罗帕酮可能导致过快心室反应而使临床加重。对于7天以上房颤国内目前能选择的药物主要为胺碘酮和伊布利特。伊布利特使用过程中患者可能出现一过性(多形)室性心律失常,一般不需要特殊处理可自行消失。该药尤以对于房扑的高转复率为临床青睐。 房颤转复后的窦律维持需要综合治疗。而抗心律失常药物方面目前可选用的有胺碘酮、普罗帕酮和施太可。胺碘酮因其较少心脏副作用而适合那些器质性心脏病人。普罗帕酮则对心脏结构正常的患者有价值。施太可归类为III类抗心律失常药物,但具有很强的β受体阻滞作用。使用过程中需注意对心功能和对气道阻力影响而产生的不良临床反应。此外,部分患者使用施太可可能发生尖端扭转型室性心律失常,这一不良反应与药物剂量有关,尤其当启用和加量时需要注意。 总之,药物治疗仍然是房颤处理过程中必不可少的选择。心室率控制是房颤处理的第一步,不但有利于稳定血流动力学,而且留给临床更多时间分辨、鉴别和思考能否立刻转复窦律(?)、是否需要抗凝(?)、有无特殊因素需要去除(?)等等。 房颤是重要的缺血性脑卒中的独立危险因素。房颤脑卒中患病率15%—20%之间,故房颤患者预防脑卒中尤为重要。目前方法包括手术治疗和药物治疗。手术如导管射频消融根治房颤、左心耳封堵术。药物传统的包括华法林、阿司匹林、氢氯吡格雷。新型药物如直接凝血酶原抑制剂和Xa因子抑制剂正在临床试验阶段,初步研究证实其具有口服方便、出血风险小、不用监测等优点。临床应根据房颤患者脑卒中危险评估(CHADS2评分)评估高危、中危和低危而药物选择。 最新研究显示经食管超声房颤发作24小时即可出现心房内血栓,故超过24小时房颤都应抗凝治疗。另外有研究显示宽松的心室率控制和严格心室率控制无明显不良差异,但次研究结果需进一步大规模研究证实。
王永军 副主任医师 河北省胸科医院 心血管内科1610人已读 - 引用 卵巢交界性肿瘤
北京大学人民医院 李艺 沈丹华 崔恒在我接到的咨询中关于卵巢交界性肿瘤的问题特别多,不仅来自患者,家属,更多的是来自专业的妇产科医生。故将我与同事李艺(她也在好大夫网站开通了咨询网页)及病理科主任沈丹华教授共同撰写的文章发表于此,仅供各位同道参阅,或也可为患者和家属解惑一、二。l 要点1. 卵巢交界性肿瘤是介于良性腺瘤与癌之间的具有恶性潜能的卵巢上皮性肿瘤。2. 病理学表现为肿瘤上皮呈复杂性增生,同时伴有细胞及结构的轻-中度的非典型性,并且这种结构应至少占到肿瘤的10%。肿瘤不出现超过微浸润范围的间质浸润。3. 肿瘤整体预后好,对于年轻有保留生育功能要求的病人,可行保守手术。无生育要求的患者,标准术式是留取腹腔冲洗液后作全子宫、双附件、大网膜、阑尾切除术、腹膜多点活检。不必常规切除盆腹腔淋巴结。4. 术后无肿瘤残留者和没有腹膜浸润的患者不必接受辅助治疗;化疗宜选用较温和的PC方案,疗程不宜过于集中。5. 最重要的预后因素是卵巢外病变的性质,II、III期患者腹膜种植的类型是主要的预后因素。术后残留病灶的大小也有预后意义。 l 发病特点卵巢交界性肿瘤病因不清,目前认为它来源于卵巢表面特化的腹膜或衍生物以及上皮包涵囊肿。流行病学调查显示未产妇比经产妇风险高,哺乳是保护因素,但口服避孕药无保护作用。其准确发病率尚不清楚,据估计近年发病率稳定在 2/100 000 妇女年。浆液性最常见(65%),其次粘液性(30%)。卵巢浆液性交界性肿瘤的发病年龄较良性浆液性囊腺瘤稍高,较浆液性癌低 10~15 岁 (分别为 45 岁和 60 岁) 。卵巢浆液性交界性肿瘤约50%为单侧性,30%双侧。而粘液性交界性肿瘤约8%双侧。30%的卵巢浆液性交界性肿瘤卵巢表面有肿瘤,66.7%有腹膜种植。绝大多数交界性肿瘤为I期(50%~80%)。与同样临床分期的卵巢癌相比,卵巢交界性肿瘤的预后要好得多。I期患者的5年生存率高达96%,其它各期平均约92%。 l 临床诊断卵巢交界性肿瘤术前诊断的准确性不高,正确的诊断主要依据病理组织学检查。一、 病理学诊断标准:长期以来卵巢交界性肿瘤的病理诊断标准一直存在不同的意见。经过30余年的探索,对其本质认识逐步深入,特别是2003年8月27~28日在美国马里兰州贝塞斯达举行的卵巢交界性肿瘤工作会议,就卵巢交界性肿瘤的某些病理学方面的分歧取得了较一致的意见。特别是引入了微乳头型浆液性交界性肿瘤、间质的微浸润、上皮内癌以及腹膜种植等病理诊断概念,为交界性肿瘤的治疗提供了依据。卵巢交界性肿瘤依据上皮类型可分为浆液性、粘液性,子宫内膜样、透明细胞、Brenner等类型,其中以前两型最为多见,下面就这两型交界性肿瘤及近些年提出的有关交界性肿瘤的病理学特征作重点概述。(一) 浆液性交界性肿瘤(SBOT)的病理学诊断:大体上,肿瘤呈囊性及乳头状生长,直径从2-25cm不等,平均10cm, 肿瘤表面可以出现外生性乳头。根据细胞及组织结构上的不同可以将SBOT分为两型:典型型SBOT和微乳头型SBOT。1. 典型型SBOT:占浆液性交界性肿瘤的 90 %,有典型的分支乳头结构, 乳头被覆多层上皮细胞,细胞核仅具有轻到中度非典型性,一般不出现核分裂像,或仅有少量核分裂像,但通常没有病理性核分裂像。可以出现间质微浸润灶,囊液及间质中常可见到沙粒体。2. 微乳头型SBOT:占浆液性交界性肿瘤的 5 %~10 %,显微镜下可见细长的“微乳头”直接从囊壁或大的纤维性或水肿性乳头上以无分支的形式产生,形成“水母头”样表现。乳头轴心含极少量或没有结缔组织,表面最常被覆立方形细胞。纤细形乳头的长至少是宽的5倍。纤维血管轴心周围围绕筛状上皮或微乳头与筛状结构相混合者也被归入此型中。在大多数病例中,微乳头SBOT可与典型SBOT并存, 因此,在一张切片中至少应出现一个由微乳头或筛状结构或二者共同构成的连续的区域,其最大径应>5mm,才能诊断为微乳头型SBOT。此外,。诊断微乳头型SBOT应注意以下两点:首先微乳头型SBOT不能出现间质微浸润,一旦出现间质浸润,就应诊断为浆液性癌。其次微乳头型SBOT中的核异型一般为轻-中度,如果出现重度的异型性则也要考虑乳头状浆液性癌的可能性。 两型SBOT,除在组织形态上有差异外,在临床预后上也有不同。多数研究认为微乳头型SBOT要较典型的SBOT更易出现浸润性腹膜种植,并且出现复发的间隔期也更短。因而,有人认为它是低度恶性浆液型癌的一种特殊类型,甚至有作者称其为非浸润性微乳头型浆液性癌。但绝大多数妇科病理学家仍将没有间质浸润的微乳头型肿瘤放在交界性浆液性肿瘤中。但值得注意的是:对于这型病变应充分取材,除外浸润性病变的出现,并且应该注意细胞核的异型性。如果忽略这两点,有可能漏诊一些浆液性癌,导致临床治疗不足(二)粘液性交界性肿瘤(MBOT)的病理诊断卵巢粘液性交界性肿瘤(MBOT)与SBOT诊断的标准一样:粘液上皮有复杂性增生,细胞及结构的非典型性要较囊腺瘤明显,并且这种结构应至少占到肿瘤的10%。肿瘤不出现间质浸润,即使出现也不超过微浸润的界限。MBOT可分为两型:肠型和宫颈内膜(Mullerian)型。肠型MBOT超过90%的病例为单侧肿物,肿瘤体积较大,平均直径为17cm.。切面呈多房性,含有水样或粘液样内容物,被膜光滑。显微镜下可见肿瘤由大小不等的囊和腺体组成,被覆的上皮为复层增生的肠型粘液上皮,可形成桥状及复层结构,并可有绒毛及乳头状突起。 即使是在同一肿瘤中,细胞核异型性的程度及核分裂象多少也有很大差异性,通常其异型性为轻度至中度,可以出现间质的微浸润。肠型交界性粘液性肿瘤的间质微浸润灶的直径为<5mm。与肠型MBOT相反,宫颈内膜型少见得多,约占MBOT的5%~15%,其与SBOT的临床、病理联系更紧密,无论是在组织结构上,还是种植的形态上都与SBOT更相似。13%~40%的肿瘤是双侧性,肿瘤平均直径为7-8cm 。大体结构上更类似于卵巢的SBOT,肿瘤可以是囊内生长,也可以是外生性结构。显微镜下肿瘤可由宫颈型粘液上皮及浆液(纤毛细胞)型上皮混合组成,常常可混有少量其他的细胞类型(如:子宫内膜样,鳞状上皮或嗜酸性细胞)。常呈现出复杂的分级乳头,上皮细胞排列成复层或丛状。核异型一般为轻度到中度,分裂像不常见,有较多的中性粒细胞浸润 。同SBOT一样,宫颈型MBOT也可显示微乳头结构,间质微浸润和淋巴结累及,但不伴发腹膜假粘液瘤。MBOT可以伴有上皮内癌,其定义是MBOT中某些区域显示癌的细胞学特征,但无间质浸润。但对其诊断的标准仍有些争议,有些研究者认为粘液性交界性肿瘤显示以下某一种或多种特征就可诊断上皮内癌:中等到高度细胞异型上皮复层达到4层或更多层、腺腔内出现筛状或出现无间质的乳头状增生。但目前一致认同的诊断上皮内癌的标准是:存在细胞学异型性应该达到重度(3级)。而对于具有过度的上皮分层和其他复杂的囊内生长结构,但细胞缺乏重度异型性,仍应视为交界性肿瘤,而不应诊断为上皮内癌。(三)腹膜种植卵巢浆液性交界性肿瘤经常伴有较高频率的卵巢外病变。大约有20%~46%的SBOT出现盆腹腔浆膜及网膜表面的种植。腹膜种植分为浸润性种植和非浸润性种植。(1)浸润性种植:组织学上表现为上皮杂乱无章的增生,不规则地延伸到腹膜下面的正常组织并将其破坏。种植灶常常由细长的乳头、腺体、小的实性细胞巢或筛状上皮巢组成。细胞一般轻度至中度异型,有时有重度异型,像高级别的浆液性癌。(2)非浸润性种植在形态学上又分为两种:有上皮增生但无间质反应的上皮性种植和伴随明显间质反应的促纤维生成性种植。上皮型的特点是:乳头状增生的浆液性上皮,位于腹膜表面或边界光滑的间皮凹陷中,其下方的组织没有被侵犯,细胞的异型性不明显,没有核分裂象,经常可以看到沙粒体。这一型的种植性病变类似其卵巢的病变。促纤维生成型特点是:增生的肉芽组织型纤维母细胞在腹膜表面形成斑块状结构,其中有小乳头、腺体和类似腺体的结构、单个细胞以及小细胞巢。有研究者认为这些腺样成分更象反应性的间皮增生。上述非浸润性种植的两种类型可同时存在。无论为何种类型的非浸润性种植,均不影响其 10 年存活率。有关腹膜种植病变究竟是真正的种植(即从卵巢肿瘤上脱落的肿瘤细胞种植到腹膜表面继续生长),还是独立于卵巢的原发腹膜肿瘤,一直存在着争议。有学者认为卵巢SBOT所合并的“腹膜种植”可能是来源于第二Müllerian系统的病变,其性质可以与卵巢病变相同,也可以不同于卵巢病变。但一些临床病理研究显示,伴有累及卵巢表面的外生性SBOT以及微乳头型SBOT的患者发生腹膜种植的危险度要高于囊内性SBOT患者,表明至少在一些病例中腹膜种植是真正的种植。不管腹膜病灶是多中心的原发病灶,还是种植后的病灶,种植的类型对于预后的判断极为重要。浸润性种植预后较差,50 %以上有复发,10 年存活率约 35 %。 Bell 等报道浸润性腹膜种植的复发率为65% ,而非浸润性种植仅 14 %复发。Seidman统计4129例交界性浆液性肿瘤经7.4年(中位数)随访,非浸润性腹膜种植者存活率可达95%,而浸润性腹膜种植者则降到66%。因此临床医生在手术时对腹腔应慎重地行多点活检来寻找病变,浆液性交界性肿瘤中发生浸润种植者是唯一的致死原因,只有这类患者需要化疗。(四)间质微浸润 卵巢交界性肿瘤可以伴有间质的微浸润,其中SBOT中出现间质微浸润的比例最高,大约有10%~15%的SBOT包含间质内微浸润灶,在妊娠病人合并浆液交界性肿瘤时,其间质微浸润的比例更高,有文献报告微浸润发生的比例可高达80%。微浸润灶非常小,通常不会引起显著的间质反应。诊断时应采用交界性肿瘤伴微浸润(borderline tumors with microinvasion)而不采用“微浸润交界性肿瘤” (”mciroinvasison borderline tumors”)一词。根据其形态学特征可将其分为三种形式:前两种主要见于SBOT, 后一种见于MBOT.第一种形态特征为:在肿瘤的乳头纤维间质或囊内间质中出现单个细胞或细胞簇、巢。这些瘤细胞轻度至中度异型,具有丰富的嗜酸性胞浆。周围间质一般正常或有轻度纤维组织增生。大部分报道的间质微浸润都属于这种类型。第二种很少见。镜下特点是:小的实性细胞巢或微乳头浸润到间质中,其周围常有清楚的空隙或裂隙。 其中还可出现筛状结构以及圆形集合性的乳头,类似浸润性低度浆液性癌。第三种: 在间质中出现单个细胞或由粘液上皮细胞组成的腺体及小簇/巢浸润;浸润灶周围常有明显的空隙,腺体不规则,边缘不整,并常伴有间质水肿、纤维母细胞增生以及炎细胞浸润。微浸润灶的大小标准尚无定论。最初提出SBOT中微浸润的诊断标准为:单一浸润灶的最大径≤3mm, 后也有人提出面积≤10mm2。在2003年交界性肿瘤会议的多数参会者更倾向于采用任何单一病灶的直径≤5mm。而对于MBOT微浸润灶的标准,尚没有统一标准,一些研究者仍采用与SBOT相同的标准,即浸润灶最大径不超过3mm, 面积不超过10mm2,但也有些研究者采用不同的大小标准,但一般认为,如果微浸润的最大径不超过5mm, 细胞的异型性未达到重度(高级别),预后都非常好。 当肿瘤主要有MBOT组成,但其中的浸润灶最大径>5mm, 可诊断为粘液性交界性肿瘤伴有粘液癌成分,并注明癌灶的大小,以提醒临床医师的关注。 (五)淋巴结受累淋巴结受累(Lymph node involvement)是指淋巴结中出现类似卵巢交界性的上皮增生,通常受累的是盆腔或主动脉旁淋巴结。据报道,在接受淋巴结取材的SBOT患者中有7-23%有区域淋巴结受累。这些病灶可能是淋巴窦中的真性转移,也可能是将窦中的间皮细胞误认为肿瘤细胞,或来源于苗勒包涵腺体的原发性卵巢浆液性交界性肿瘤。因而尚不能确认淋巴结受累是与卵巢肿瘤具有克隆性关系还是独立性的病变,而且具有淋巴结受累的患者并未影响其预后。Seidman统计43例交界性浆液性肿瘤伴淋巴结转移者,经6.5年(中位数)随访,存活率达98%。因此,建议不使用 “淋巴结转移”这一名词,而是使用“淋巴结受累”来描述此类病变。(六)腹膜假粘液瘤腹膜假粘液瘤((Pseudomyxoma peritonei, PMP)是指在手术中发现盆腹腔内出现大量粘液腹水和/或在腹膜表面有多量粘液结节,通常还伴有卵巢和阑尾的粘液性肿瘤。以往认为,PMP是由原发卵巢粘液性肿瘤,尤其是肠型MBOT破裂后播散到腹膜而形成。但最近的形态学、免疫组化和分子遗传学研究都提供了强有力的证据,表明实际上几乎所有的PMP都起源于胃肠道,尤其是阑尾粘液性肿瘤,而与PMP同时存在的卵巢肿瘤是继发性的。PMP以往是作为诊断名词使用。现认为PMP只是一种临床描述,而不是一个病理诊断。对于腹膜假粘液瘤的患者,应注意检查阑尾,并应对腹膜假粘液瘤标本作全面的组织学检查,对其中出现的上皮成分进行分级:即良性、交界性或恶性。二、临床特征 患者一般无特殊症状。随着肿瘤增大可表现为腹部不适、胃肠道症状、泌尿系压迫症状。若肿瘤破裂,可出现急腹症表现。部分患者为妇科查体发现。三、肿瘤标记物 浆液性交界性肿瘤常用的血清肿瘤标记物是CA125,Gotlieb 回顾分析了91例患者,75%浆液性交界性肿瘤患者术前CA125升高,平均为156IU/ml;而粘液性仅30%升高,平均为28IU/ml。而且CA125水平与肿瘤分期相关。Ia期患者仅有35%升高,平均67 IU/ml;有卵巢外播散者则高达89%升高,平均259 IU/ml。 CA19-9是一种肿瘤相关性抗原,一般多见于消化系肿瘤。Engelen报道粘液性交界性肿瘤有57%术前CA19-9升高,因此推荐CA19-9作为粘液性肿瘤的肿瘤标记物。CA19-9同时可用于监测病情,建议粘液性肿瘤随访用CA19-9,早期发现复发。CEA在交界性肿瘤中阳性率仅7.7%~9%,对于诊断无特异性。四、影像学检查 彩色超声检查是重要的辅助检查手段。卵巢交界性肿瘤的声像诊断:首先要有囊内复合体(即乳头或房隔)、PI<1.0、缺乏肿瘤内汇合血管;结合CA125<150U/L,年龄<60岁,其诊断准确率可达91%。迄今为止,交界性肿瘤的最常见的两个特征声像仍是囊内乳头结构和多房隔,但不是诊断的敏感指标。尽管其阳性预测值和敏感性较差,但是特异性和阴性预测值高。最近Exacoustos回顾分析了33例交界性肿瘤患者的彩超资料,并与82例恶性、337例良性患者进行对比,发现交界性患者48%有小乳头结构,即乳头的基底宽度<10mm、高度<15mm,24%有房隔结构;而恶性患者更多表现为纯实性或囊实性肿物,囊内乳头基底宽度多>10mm、高度多>15mm;良性肿瘤多为单房、囊壁光滑、直径<5cm的囊肿。交界性肿瘤仅9%为单房囊肿,恶性没有单房囊肿。肿瘤的内部,特别是乳头内部出现血流信号在交界性肿瘤和恶性更多见,分别是56.3%和66.7%,而良性没有一例有血流信号。同时交界性和恶性肿瘤比良性肿瘤更多出现低阻力血流信号,但二者间没有区别。如果特征声像结合血流情况,其特异性可高达100%,但敏感性下降到27%。 Fruscella 进一步指出不同病理类型交界性肿瘤声像特征仍有区别。浆液性肿瘤和粘液性肿瘤中的宫颈内膜型具有较相似的特点:肿瘤体积较小,囊腔少(通常为单房)、囊内多有乳头或实性区、乳头内部血流低阻(RI<0.4)者多。而粘液性肿瘤中的肠型的特点是:单侧、肿瘤体积大、多房隔(>10个囊腔者多)、囊壁光滑、囊内实性区或乳头少(图57-13)。五、冰冻病理诊断鉴于交界性肿瘤术前诊断率仍不高,术中冰冻病理显得非常重要。冰冻病理的可靠性各家作者报道不一,尤其对粘液性交界性肿瘤。一般认为鉴别良恶性较可靠,但鉴别交界性与恶性或交界性与良性则不是非常准确。Wong报道200例冰冻病理的结果,22%粘液性交界性肿瘤误诊为良性,而浆液性交界性肿瘤的误诊率为5%。对粘液性肿瘤的误诊率高,主要是粘液性肿瘤的异质性造成的。鉴于冰冻病理的局限性,术中根据冰冻病理结果决定手术范围仍具有相当的风险性。术前与患者和术中及时与家属的沟通是十分明智的。l 诊治流程可疑交界性卵巢肿瘤的患者,先进行血清CA125和CA19-9检查,以及阴道彩超检查。术中送冰冻病理检查。有生育要求的患者实行保守手术,无生育要求患者的标准术式是留取腹腔冲洗液后作全子宫、双附件、大网膜、阑尾切除术、腹膜多点活检。不必常规切除盆腹腔淋巴结。术后无肿瘤残留者和没有腹膜浸润的患者不必接受辅助治疗。l 卵巢交界性肿瘤治疗方法选择的原则卵巢交界性肿瘤的治疗主要为手术治疗,除特殊病例外,现多不主张加用辅助治疗。一、卵巢交界性肿瘤的保守性手术 约1/3的卵巢交界性肿瘤患者年龄小于40岁,很多病人有保留生育功能的要求。大量的临床研究结果提示保守手术患者的无病生存率和总生存率与进行了满意的分期手术的患者无区别,都接近100%。而且保守手术后患者的生育、妊娠结局也很好,但术后需严密随访。保守性手术通常指患侧附件切除,适用于年轻、有生育要求的患者。手术应满足以下条件:①患者年轻、渴望生育;②确定为I期、对侧卵巢和输卵管正常;③术后有条件长期随访。年轻患者如一侧卵巢有肿瘤时,一般开腹后留取腹水或腹腔冲洗掖,然后先作一侧附件切除, 剖视有可疑时送冰冻切片。如病理报告为交界性卵巢肿瘤,对侧卵巢应作剖视,并送病理检查,同时应仔细探查盆腔及上腹部,如均无恶性证据,可不再作其他手术。由于附件切除和囊肿剥除术后的复发率分别是2-3%和20%,因此囊肿剥除术仅限于双侧交界性卵巢肿瘤或已有一侧卵巢切除的患者。切除标本应每1~2cm做一切片检查,明确是否无侵袭。术后石蜡切片病理检查如为癌,可根据情况进行卵巢癌再分期手术和/或加用化疗。 Kennedy等探讨了有卵巢外病变或晚期患者行保守手术的可能性。76例交界性浆液性肿瘤患者,39/76例有卵巢外病变,28/74例为II或III期患者,其中66例随访了8~264个月(平均99个月)。仅有1/66例(1.5%)病情进展,死于广泛播散的浆液癌;2/18(11.1%)例行保守手术者复发。长期随访显示:卵巢外病变并不意味着腹膜种植,对年轻患者行保守手术是可行的。有作者报道交界性肿瘤患者行子宫+双附件切除、附件切除和单纯囊肿切除术后的复发率分别为5.7%、15.1%和36.3%。复发后可再次行保守手术,仍可获得妊娠和长期存活。特别在有生育要求的患者保守手术方式中,单纯卵巢囊肿剥除术似乎也是适合的选择。Yinon比较了40例附件切除和22例卵巢囊肿剥除术的结果,平均随访88个月。两组患者肿瘤复发率无差异,分别是27.5%和22.7%;但是囊肿剥除组患者无瘤间期明显短于附件切除组,分别是23.6和41个月(无统计意义)。共25例患者获得妊娠38次,分娩35次。综上所述认为保守手术的复发风险虽然显著升高,但不影响最终的生存率。生育问题是保守手术后值得关注的问题。Morice综述大约10-35%的患者术前即存在不孕问题,保守手术术后自然妊娠率32-65%,对持续不孕的病例可选择试管婴儿助孕。年龄与妊娠率密切相关,<35岁者妊娠率42%,35-40岁降为22%,>40岁没有妊娠。促排卵药是否增加癌变还有争议。目前认为早期交界性肿瘤保守手术后促排卵治疗是安全的。在晚期或微乳头型患者最好不要应用促排卵+IVF,以免加速疾病进展。Fortin 报道了30例交界性肿瘤的不孕症患者术后接受促排卵治疗,平均周期2.6个,中位随访时间93个月,在随访42个月时有4例复发(3例单纯卵巢囊肿切除术)。所有复发病例仍然为交界性肿瘤,通过再次手术治疗。目前所有患者无瘤生存,共有13例妊娠。保守手术后随访非常重要,保守手术后2年内,每3月复查一次,以后每半年一次。5年时复发率可达20%,即使妊娠分娩后也要随访。分娩后是否切除卵巢有争议,需考虑多个因素:肿瘤组织类型、分期、保守手术的术式以及病人的意愿。目前认为对能常规随访的患者不必推荐切除卵巢,只有复发时再切除。有些病人因心理因素或想简化随访程序而在产后要求切除卵巢。在交界性肿瘤的手术中对侧卵巢的楔形活检问题值得注意。浆液性与粘液性交界性肿瘤均可以双侧发生,许多作者建议对健侧卵巢行楔形活检;但也有人反对,认为术后易出现卵巢周围粘连而导致不孕。虽然目前微创技术和抗粘连制剂的应用能减少粘连的发生,但有报道肉眼外观正常的卵巢,镜下分析也无病灶,因此对对侧卵巢活检的价值提出疑问。目前尚无统一意见。既往主张在完成生育功能后切除保留的卵巢,现在认为可以继续保留。二、卵巢交界性肿瘤的其他手术临床I期成年人如不再需要生育时, 标准术式是留取腹腔冲洗液后作全子宫、双附件、大网膜、阑尾切除术、腹膜多点活检。由于常常在同一肿瘤中同时存在良性、交界性和恶性成分,如术中冰冻切片病理检查不能确定交界性或恶性,则一般应进行淋巴结清扫;II、III、IV期者可行肿瘤细胞减灭术。对于较晚期患者应行肿瘤细胞减灭术,但淋巴结是否切除值得质疑,因为它与生存期无关。临床治疗达到完全缓解的患者现多主张不进行二次探查术。三、腹腔镜手术既往认为腹腔镜处理交界性肿瘤尚不成熟,术前考虑到交界性肿瘤者不主张行腹腔镜手术,避免种植。随着腹腔镜技术的进步,研究病例的增多,目前认为可选择合适的病例安全有效地进行腹腔镜手术。Vaisbuch 综述了腹腔镜处理交界性肿瘤的历程,2003年后陆续报道多家医疗中心分别成功完成30例、24例、34例腹腔镜手术,认为腹腔镜手术治疗交界性肿瘤是安全、有效的。Desfeux报道了48例腹腔镜手术病例,尽管术中肿瘤破裂几率增加,但与开腹手术患者的生存率无差别。一项意大利的多中心研究共纳入113例交界性肿瘤患者,其中52例腹腔镜手术,其余开腹手术。肿瘤直径2-30cm。腹腔镜术中破裂和渗漏比例高达34%,而开腹仅7%(差异有显著性)。复发率11.5%,但与手术路径无关,也不影响预后。Maneo分析腹腔镜术后病变持续存在与肿瘤大于5cm有关,病理为浆液性、分期为Ic以及行卵巢囊肿剥除术似乎都与病变有关。因此腹腔镜手术似乎更适合于年轻、肿瘤小于5cm、有生育要求而行保守手术的早期患者,可以减少术后粘连,有利于术后怀孕。为减少复发,保守手术最好选择切除患侧附件。如果病变为双侧卵巢,才考虑囊肿剥除术。腹腔镜处理妇科恶性肿瘤的穿刺口转移率一般在约1%,与开腹手术无差别;交界性肿瘤术后穿刺口转移仅有个案报道,因此穿刺口种植问题不应该成为反对腹腔镜的理由,转移诊断后需要手术切除。腹腔镜手术中注意的事项:需要技术熟练的医师,手术开始先留取腹腔冲洗液,仔细探查双侧卵巢和整个腹腔,可疑处送冰冻病理。术中如果肿物破裂,要彻底冲洗。建议使用取物袋。要避免术中对卵巢进行穿刺、活检或切碎的操作。但是当肿瘤放置到取物袋内后,可以进行穿刺抽吸。四、卵巢交界性肿瘤是否需要再分期手术对于初次治疗未行分期手术的患者,是否在病理确诊后需要进行再分期开腹手术是临床医师关心的问题。Winter 分析了48例传统分期手术与45例未分期手术的患者,发现尽管17%术后分期升级,但5年总生存率及复发率是没有区别的。Rao对183例患者的资料分析,也认为交界性肿瘤患者不必常规行盆腔和腹主动脉旁淋巴结清扫。因此,目前认为对初次未分期手术没有大体残留病灶的患者,尽管再分期手术会“升级”,但是这对治疗是否有益处值得疑问。五、辅助治疗 超过I期的患者,是否需作辅助化疗,各家意见还不十分一致。有文献报道,辅助治疗不仅不能改变交界性肿瘤患者的预后,过度化疗可引起并发症,增加患者的死亡率。尚无任何前瞻性随机研究支持化疗有益。但也有报道交界性肿瘤对化疗并非完全不敏感,术后辅助治疗仍有一定的近期疗效。特别是术后有残留病灶者,化疗可使肿瘤松动、病灶缩小,待条件许可时再次手术,可达到将肿瘤完全切除的目的。因此,关于交界性肿瘤的术后辅助治疗,提出以下几点:①应明确交界性肿瘤辅助治疗的目的是缩小病灶,有肿瘤残留者可给予化疗,为再次减瘤手术成功创造条件,但不能期待利用辅助治疗改善预后;②FIGO I期及其他期别术后无肿瘤残留者,不必接受辅助治疗,但应严密随访;③没有腹膜浸润的患者不需要辅助治疗,浆液性交界性肿瘤中只有发生浸润种植者需要化疗;④交界性肿瘤的肿瘤细胞增殖速度较上皮性癌缓慢,化疗应有别于卵巢上皮癌,宜选用较温和的方案,如PC方案较为理想,疗程不宜过于集中;⑤建议开展肿瘤细胞DNA含量、倍体水平及有关癌基因的检测,明确转移灶的病理类型,使治疗有的放矢。l 随访与影响预后的因素卵巢交界性肿瘤应象卵巢癌一样进行随访。阴道超声、妇科检查及血清标记物是患者术后随访的常规项目,其中阴道超声检查是目前发现复发最有效的手段。浆液性交界性肿瘤用CA125,粘液性肿瘤随访用CA19-9。最重要的预后因素是卵巢外病变的性质,II、III期患者腹膜种植的形态学是主要的预后因素,预后不良者显示以下3种特征之一:微乳头型,被裂隙围绕的实质上皮巢,浸润其下方组织。浆液性交界性肿瘤伴微乳头型预后差,10年生存率仅60%。如Ayhan分析了100例交界性肿瘤病例,发现小于30岁行保守手术、有微乳头结构或腹膜种植者的无病生存率显著降低。腹膜种植的类型决定患者的预后,伴有浸润性腹膜种植的患者预后差。术后残留病灶的大小也有预后意义,初次手术后有残留病灶是预后不良的指标。无残留病灶的患者影响预后的独立因素有:DNA倍体,形态测定,FIGO分期,组织学类型和分级,年龄。特别是DNA倍体和形态测定可作为指导预后的指标。交界性肿瘤非整倍体者生存率仅15%。而手术方式和化疗不是独立的影响因素。来自瑞典的399例患者的队列研究显示,其中63例肿瘤DNA非整倍体,大多数辅以化疗。经长达11年的随访,累积相对5年和10年生存率分别是99.9%和103.5%。非整倍体在大于60岁的患者多见;而且似乎粘液性肿瘤比浆液性肿瘤更多见(无统计意义)。
崔恒 主任医师 北京大学人民医院 妇科6.4万人已读 - 引用 ALK基因及突变的简介
该基因最早发现于间变性大细胞淋巴瘤,因此得名ALK(anaplastic lymphoma kinase,间变性大细胞淋巴瘤激酶)。后来在多个癌症中发现,是强力的致癌驱动基因。ALK蛋白位于细胞膜上,胞外是受体区,胞内为激酶区,正常情况下经细胞外的配体将2个ALK蛋白偶联后激活胞内信号通路,促进细胞生长。其作用机制和ALK突变后异常激活与EGFR的机制相似。ALK基因的突变类型有3种:1、融合突变是ALK最常见的突变,基因融合后所表达出的蛋白就好比给绿皮车厢加上了高铁火车头,表达异常活跃2、点突变 相对少见,主要发生在胞内激酶区,打了鸡血的ALK不停地给下游通路传达细胞生长的信号3、扩增突变也相对少见,通过增加与配体结合进而偶联的机会,提高促进细胞生长的信号ALK在很多肿瘤中均有发现,在NSCLC中,以EML4-ALK融合突变为主,EML4-ALK融合有不同的融合亚型。ALK的点突变,主要是守门员基因的突变,与ALK抑制剂的耐药有关。
王颖轶 主任医师 北京协和医院 肿瘤内科5.7万人已读 - 引用 间变性大细胞淋巴瘤的治疗
1982年Stein发现Reed-Sternbeng细胞示CD30(Ki-1,Ber-H2特异性单抗)阳性,后来在部分非霍奇金淋巴瘤(NHL)亦见到Ki-1阳性细胞,称之为Ki-1阳性大细胞淋巴瘤.并显示多形性大细胞增殖,特有的副皮质生长类型,局部坏死和显著的窦状隙弥散的病理学特征,而称之为间变性大细胞淋巴瘤(anaplastic large cell lymphoma, ALCL),成为具有共同的临床病理学特征的实体.这些病例原先已被诊断为恶性组织细胞增生症或间变性癌。间变性大细胞淋巴瘤(Anaplastic Lagre Cell Lymphoma,简称ALCL)是一种较少见的侵袭性非霍奇金淋巴瘤。因强烈表达细胞因子受体Ki-1(CD30),曾有“Ki-l淋巴瘤”或Ki-1阳性大细胞淋巴瘤之称。近年来随着免疫组化的应用和分子生物学技术的发展,对ALCL的认识有了很大提高。2001年新的WHO淋巴瘤分类将ALCL定义为:间变性大细胞淋巴瘤(ALCL)是一种T细胞淋巴瘤,瘤细胞常较大,具多形性,胞浆丰富,常有马蹄形的核,瘤细胞CD30阳性,大多数病例表达细胞毒性颗粒相关蛋白。大多数病例ALK阳性,但ALK阴性的病例也包括在内。原发系统型ALCL必须与原发皮肤型ALCL及其它有间变性特点且表达CD30的T或B细胞淋巴瘤鉴别开(文中如未提到细胞来源,则特指T/裸细胞ALCL)。2.1 ALCL的临床病理学特点2.1.1 流行病学特点新的WHO分类中统计ALCL约占成人非霍奇金淋巴瘤的3%,占儿童淋巴瘤的10-30%,是儿童外周T细胞淋巴瘤中最常见的一种类型,占大细胞非霍奇金淋巴瘤的比率少于2%。ALCL的发生有两个高峰。ALK阳性的 ALCL常发生于生命的前三个阶段(0-9、10-19、20-29岁),且男性多于女性,尤其是在第二(10-19岁)、三(20-29岁)年龄段性别差异更明显(男:女=6.5:l)。ALK阴性的ALCL常发生于老年人,男女比率无明显差异(男:女-0.9:l)。2.1.2 形态学特点ALCL大体标本多为均一新鲜鱼肉状肿物,可破坏部分或全部淋巴结结构。有结外病变者,常表现为相应部位的肿物。如发生于皮肤,常表现为皮肤斑丘疹、单发或多发小结节、皮下肿块等,皮肤表面可有溃疡形成;如发生于骨组织,常可见溶骨性破坏等。瘤细胞在组织学上有一特征性的生长方式,即其沿淋巴窦和滤泡间浸润。在部分受累的淋巴结,可有淋巴滤泡和淋巴窦残存。另外瘤细胞还常呈一种黏着性的生长方式,除散在分布外,细胞有形成团块状倾向或形成巢状。此特点使ALCL有时很象转移性肿瘤。ALK阳性ALCL,其瘤细胞的形态学范围较宽。但所有病例都有不同比率的形态古怪、有着肾形或马蹄形核的细胞,靠近胞核常有一个嗜酸性区域。这些细胞被称之为ALCL的特征性细胞(hallmark cell),因为在所有形态学类型的ALCL病例中都可见到。尽管典型的特征性细胞体积大,但有着相似的细胞学特点的小细胞也可见到,且对ALCL的正确诊断有很大帮助。2.1.3 免疫学特点所有ALCL病例均强表达CD30,阳性信号位于胞膜和高尔基器(Gologi)区域(弥漫的胞浆表达意义是可疑的)。这是很多研究者在对大量大细胞肿瘤进行CD30检测时发现的结果。因此膜相关的CD30阳性表达被写进ALCL的定义内[5]。ALK在60-85%的 ALCL病例有表达。大多数 ALCL病例EMA阳性。大多数ALCL表达一种或多种T细胞抗原,然而,由于全T细胞抗原的丢失,有些病例可以表现一种明显的“裸细胞”(null cell)表型[4]。2.1.4 遗传学特点无论是否表达T细胞抗原,大约90%的病例有T细胞受体(TCR)基因重排,多数为TCRβ、TCRγ基因重排。ALK的表达是由于位于2号染色体的ALK基因的改变。研究者发现在大约60-85%(53-89%)的 ALCL病例有反常ALK蛋白的表达。2.2 临床表现临床上,ALCL可区分为原发性和继发性,后者从其他淋巴瘤转化而来。原发系统型ALCL占成人NHL的5%,占儿童大细胞淋巴瘤的20-30%。系统型间变性大细胞淋巴瘤ALK阳性和阴性的比例分别为60%和40%,ALK阳性和阴性的系统型ALCL的临床特点和预后不同。 2.2.1 ALK阳性系统型ALCLALK阳性系统型ALCL大部分发生于30岁以内,男性多见,男女比为1.2-2:1。常表现为外周或腹部淋巴结肿大,大肿块多见,占30-54%。40%的病人为弥漫性广泛浸润,常伴腹股沟淋巴结受侵。纵隔受侵比 HD少见,25%的病人有脾肿大。43-63%的病人为Ⅲ/Ⅳ期并伴B组症状,高热和体重下降常见。60%的病人有结外受侵,而多个结外部位受侵占40%,皮肤(21%)、骨(17%)和软组织(17%)是最常见的结外受侵部位,胃肠道和中枢神经系统受侵极少见。和HD不同的是,ALCL较少侵犯纵隔。表达NPM-ALK和其他ALK融合蛋白ALCL的临床表现和预后无差别。在儿童ALCL,ALK阳性率更高。2.2.2 ALK阴性系统型ALCLALK阴性系统型ALCL的病理形态、免疫表型、临床表现和ALK阳性系统型ALCL基本相似,主要区别为 ALK阴性,发病年龄较大,预后差。霍奇金样ALCL常发生于年青人,85%的病人为ALK阴性,常为IIA期,约60%的病人表现为大纵隔,但无皮肤和骨受侵[8]。这些临床表现和 ALK阳性系统型 ALCL有较明显差别。2.2.3 原发皮肤型ALCL原发皮肤ALCL定义为病变局限于皮肤,未见全身受侵,无蕈样霉菌病、外周T细胞淋巴瘤、淋巴瘤样丘疹病或HD病史。病变位于皮肤和区域淋巴结受侵时,鉴别诊断困难。原发皮肤ALCL占皮肤淋巴瘤的10%,中位发病年龄60岁。和ALK阳性系统型ALCL不同的是,皮肤ALCL的ALK为阴性,缺乏细胞毒基因表型。预后好,临床病程多为惰性。临床表现为单发、无症状的皮肤或皮下紫红色结节,表面常可破溃。多发结节少见。常发生于四肢和躯干。约25%的病人可出现部分或完全性自发性肿瘤消退。根据WHO分类原则,原发系统型ALCL和原发皮肤型ALCL是两种独立的病理亚型,其临床表现和预后明显不同(表1),两者是不同的病种。原发系统型ALCL为侵袭性,需全身化疗,而原发皮肤型ALCL表现为惰性,仅需局部治疗。原发皮肤型ALCL常需和淋巴瘤样丘疹病鉴别,其临床特点和病理特点鉴别如下。 2.2.4 继发性ALCL继发性ALCL从其他淋巴瘤如蕈样霉菌病、外周T细胞淋巴瘤、HD或淋巴瘤样丘疹病发生间变转化而来,常为老年,ALK阴性,预后差。2.4 治疗和预后 原发系统型ALCL的治疗以化疗为主要治疗手段,辅以放疗。早期ALCL行化疗后做受累野放疗,晚期以化疗为主。大多数报道以联合化疗为主,成人用中高度非霍奇金淋巴瘤治疗方案(多采用含有阿霉素的方案如CHOP和MACOP-B等),儿童用淋巴母细胞淋巴瘤或Burkitt淋巴瘤治疗方案。大多数报道的病例均有很高的完全缓解率(70-95%),复发病例一般对化疗仍然敏感。 Shiota等最早于1995年报道了 ALK阳性和阴性ALCL的5年生存率分别为80%和33%,在此后的研究中证实了ALK阳性ALCL的预后明显优于ALK阴性ALCL,5年生存率分别为 71-95%和15-46%。表5比较了最近几年报道的 ALK阳性和阴性系统ALCL的临床表现和治疗结果。在儿童和年青病人的侵袭性NHL中,ALK阳性系统型ALCL治愈可能性最大,预后优于任何其他形式的外周T细胞淋巴瘤。
张明智 主任医师 郑大一附院 肿瘤科1.1万人已读 - 引用 淋巴结肿大与淋巴瘤
淋巴结是外周免疫器官,是淋巴细胞增殖与分化的场所,正常淋巴结很小,直径多在0.2-0.5cm,呈豆形或椭圆形,质地柔软,扁平,表面光滑,无压痛,与周围组织无粘连。正常人浅表淋巴结除颌下、颈、腋下及腹股沟外,一般均不易触及。如果浅表淋巴结超过1.5cm,外形改变,质地异常称为淋巴结肿大。淋巴瘤是起源于淋巴结和淋巴组织的恶性肿瘤,属于免疫系统恶性肿瘤。多年于青年人,首发临床表现常是无痛性颈部或锁骨上淋巴结进行性肿大,其次是腋下淋巴结肿大,肿大淋巴结可互相粘连,融合成块,触诊有软骨样感觉(像触摸自己的额头),无痛性进行性淋巴结肿大或局部肿块是淋巴瘤共同的临床表现,同时可有相应器官压迫症状,淋巴结、扁桃体、脾脏及骨髓是最容易受到累及的部位。全身发热、盗汗、瘙痒及消瘦症状多见,饮酒后淋巴结疼痛是霍奇金淋巴瘤患者特有的临床表现,由于每个患者的病变部位和范围都不相同,所以临床表现具有多样性。局部淋巴结肿大,需要与淋巴结炎和恶性肿瘤淋巴结转移鉴别,淋巴结炎,常有淋巴结肿大伴有疼痛,肿大淋巴结周围有炎性病变,比如上呼吸道感染、牙龈炎、鼻窦炎引起颈部淋巴结肿大,恶性肿瘤转移,一般会有原发恶性肿瘤的表现,比如鼻咽癌、甲状腺癌、胃癌、肺癌颈部或锁骨上淋巴结转移。淋巴结肿大需要综合判断,不能单一因为淋巴结肿大就怀疑恶性疾病,给自己造成紧张心理,影响生活。本文系杨华医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
杨华 副主任医师 中日医院 普外科·胃肠外科5300人已读





